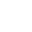醫療器械udi控制程序設計開發
作者:兆信股份 發布時間:2020.07.09 來源:http://m.lysgsy.com
DA法規要求,III類醫療器械必須帶有UDI標簽。III類醫療器械在美國是被嚴格監管的“高風險”設備,如延續或維持生命的機器,像心臟起搏器和心臟瓣膜等由FDA批準才能用于人類的醫療設備,也包括那些構成潛在危害的設備。國家藥監局表示,通過建立醫療器械udi控制程序,有利于運用信息化手段實現對醫療器械在生產、經營和使用各環節的快速、準確識別,有利于實現產品監管數據的共享和整合,有利于創新監管模式,提升監管效能,有利于加強醫療器械全生命周期管理,實現政府監管與社會治理相結合,形成社會共治的局面,進一步提升公眾用械安全有效的保障水平。
醫療器械udi控制程序設SaaS服務的軟件,符合UDI標準,是支持GS1 EPC Gen 2的無源RFID解決方案,使用斑馬的掃描儀和打印機對RFID標簽進行UDI標準編碼,過程驗證,打印所需的標簽,并登記數據到FDA UDI數據庫。
醫療器械udi控制程序即充分利用人力和機器可讀的UDI標簽對分配和使用的醫療器械進行確認識別。如對設備貼標必須要把關于每個設備的信息提交到FDA全球UDI數據庫為醫療器械制造商和醫院客戶提供符合美國食品和藥物管理局(FDA)唯一的設備標識(UDI)規定的RFID解決方案醫療器械udi控制程序
醫療器械udi控制程序設計集成到現有的UDI的數據源,或者可作為一個獨立的解決方案安裝。醫療器械udi控制程序設計可與任何符合RFID標準的標簽或擴展用戶標簽存儲數據的UDI(512字節)配合使用。
醫療器械唯一標識(unique device identifier;UDI):基于標準創建的一系列由數字、字母和/或符號組成的代碼,包括產品標識和生產標識,用于對醫療器械進行唯一性識別。
醫療器械唯一標識數據載體(unique device identifier data carrier):存儲或者傳輸醫療器械唯一標識的數據媒介;醫療器械唯一標識數據庫(unique device identification database;UDID):儲存醫療器械唯一標識的產品標識與關聯信息的數據庫;醫療器械唯一標識系統(unique device identification system;UDIsystem):由醫療器械唯一標識、醫療器械唯一標識數據載體和醫療器械唯一標識數據庫組成的醫療器械統一識別系統。
產品標識(device identifier;UDI-DI):特定于某種規格型號和包裝醫療器械的唯一性代碼。注:產品標識可用作對醫療器械唯一標識數據庫存儲信息的“訪問關鍵字”,關聯醫療器械產品信息、制造商信息、注冊信息等。
生產標識(production identifier;UDI-PI ):識別醫療器械生產過程相關數據的代碼。注:根據實際應用需求,生產標識可包含醫療器械序列號、生產批號、生產日期、失效日期等。其它“一維碼”“二維碼”“射頻識別”等術語見YY/T1681-2019標準。來源:YY/T1630 — 2018 醫療器械唯一標識基本要求;YY/T 1681 — 2019 醫療器械唯一標識系統基礎術語。
廠家和醫院可以立即通過UDI數據對醫療設備提供跟蹤,并能與制造商提供的臨床系統,計費系統和電子健康記錄(EHR)集成。在RFID標簽上的UDI數據可以讓用戶找到和召回即將到期的產品。醫療器械唯一標識的價值在于應用,各環節的有效應用是形成監管大數據的基礎,是實施互聯網+監管、智慧監管的重要途徑和手段。因此,《規則》鼓勵各相關方積極在醫療器械生產、經營和使用環節的管理中應用醫療器械唯一標識。
了解更多兆信股份醫療器械udi控制程序 ,目前,全國已經有多個家企業使用醫療器械udi控制程序, 醫療器械udi控制程序幫助企業實現大數據防偽追溯管理體系,進一步的了解可以4001102365,兆信股份醫療器械udi控制程序軟件服務,咨詢可獲得醫療器械udi控制程序解決方案;

<上一篇:
一物一碼或成母嬰市場新一代防偽營銷利器
下一篇:>
化妝品行業新規發布,四大亮點引關注